NUTRIMEME
NUTRIMEME

Infografía: Alimentación perceptiva

Tomado de: www.laspghan.org
ESTREÑIMIENTO
ESTREÑIMIENTO

El estreñimiento es una enfermedad frecuente en la consulta pediátrica, puede iniciar durante el primer año de vida, particularmente concomitante con el comienzo de la alimentación complementaria. Para su diagnóstico, cuando el estreñimiento es funcional, nos basamos en los criterios Roma IV
El estreñimiento intratable es aquel que no responde al tratamiento convencional al menos por 3 meses. La impactación fecal se identifica al examen físico, con la palpación de una masa dura en el abdomen inferior o al tacto rectal evidencia del recto dilatado con heces o en la Rx de abdomen heces excesivas en el colon distal.
Para Gastronutriped es el primer motivo de consulta con un 33%, puedes leer esta investigación en nuestra página web, www.gastronutriped.como , en la sección publicaciones .
Infografía: Intolerancia a la lactosa

Tomado de: www.nestlenutrition.org
Infografía: Microbiota intestinal

Tomado de : www.gutmicrobiota.com
Infografía: Inicio de alimentación complementaria
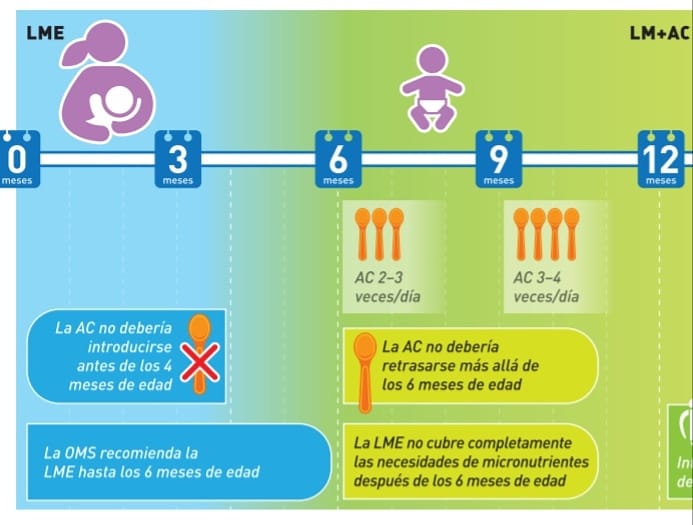
Tomado de : www.nestlenutrition.org

 Encuentre nuestra ubicación y la información de contacto.
Encuentre nuestra ubicación y la información de contacto.